Alberto Mantovani, immunologo di fama mondiale, spiega perché il lavoro di Bruce Beutler, Jules Hoffmann e Ralph Steinman cambierà le nostre vite (e quelle di milioni di bambini nel mondo). «E’ l’ultimo atto di un sogno iniziato 100 anni fa»
Bruce Beutler, Jules Hoffmann e Ralph Steinman hanno ricevuto il Premio Nobel per la Medicina. Chi sono e perché hanno meritato il premio? Lo spiega Alberto Mantovani, immunologo come i neo-Nobel, docente all’università di Milano e direttore scientifico dell’Istituto clinico Humanitas di Rozzano (Milano).
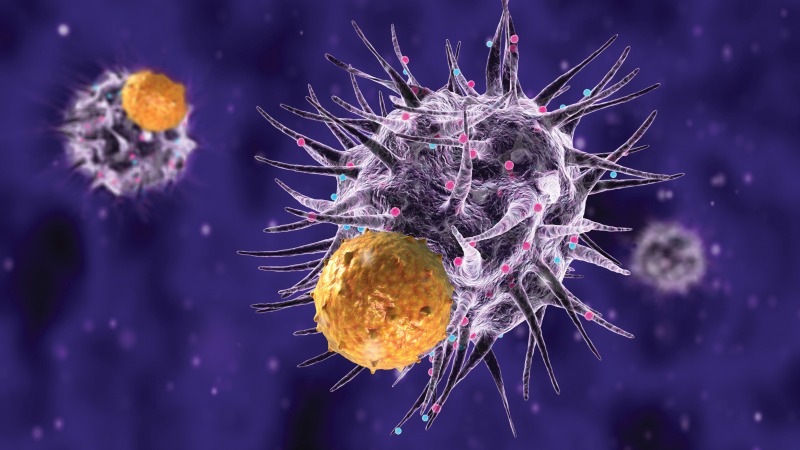
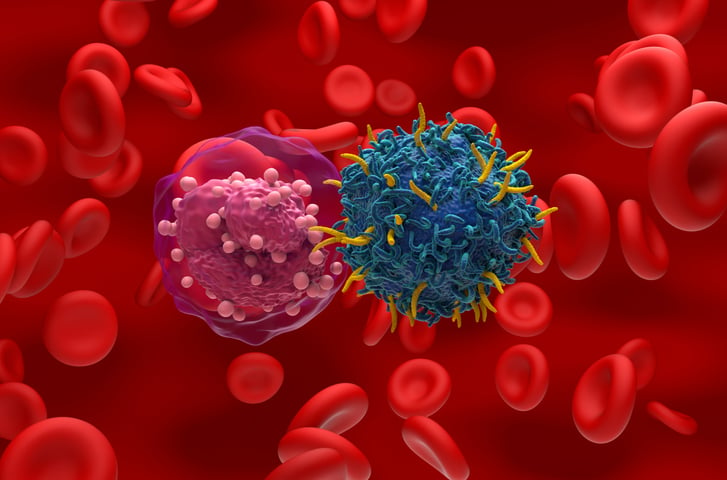
LE CELLULE DENDRITICHE - Si deve a Ralph Steinman, appena scomparso, la scoperta delle cellule dendritiche. «Sono cellule-sentinella scoperte negli anni ’70, sono un po’ ovunque nell’organismo, allertano il sistema immunitario specifico della presenza di patogeni e orientano la risposta, a seconda della minaccia (affrontare un tumore o un virus richiede armi diverse)» spiega Mantovani.
L’IMMUNITA’ INNATA – «E’ il nostro primo meccanismo di difesa. Beutler e Hoffman hanno dato un contributo fondamentale all’identificazione dei “sensori” che vengono usati dalle cellule del sistema immunitario per percepire la presenza di patogeni. Appartengono alla famiglia dei Toll-like receptors (Tlr), recettori simili a Toll» (che una ricercatrice tedesca, Christiane Nüsslein-Volhard, premio Nobel 1995, scoprì nella drosophila, il moscerino della frutta, esclamando per la sorpresa: Das ist ja toll, ovvero Questo è fantastico!).
PERCHE’ IL PREMIO - Come hanno cambiato la medicina (e la nostra vita)? «Gli studi sui Tlr hanno cambiato il modo in cui leggiamo la malattia (e non solo malattie legate al sistema immunitario). Ad esempio, sappiamo che le patologie cardiovascolari sono sostenute da una reazione infiammatoria, è cambiato il modo in cui vediamo il rapporto fra infiammazione e cancro» precisa Mantovani. «L’attivazione delle cellule dendritiche è alla base del funzionamento dei vaccini, che sono il contributo più grande alla salute dell’uomo – prosegue -. I vaccini hanno bisogno di una sostanza “adiuvante” per migliorare la risposta immunitaria. Fino a pochi anni fa si usavano adiuvanti scoperti nel 1920. La scoperta delle cellule dendritiche e dei Tlr, invece, hanno aperto la strada verso sostanze nuove come accade ad esempio con uno dei vaccini contro il papilloma virus (Hpv) o in terapie anticancro. Si è inoltre aperta la possibilità di usare le stesse cellule dendritiche come vaccino terapeutico, “caricandole” contro la malattia».
VACCINI CHE CURANO - Parliamo di vaccini non più soltanto preventivi. «Esatto. Ci sono studi in tutto il mondo, al momento il risultato clinico è l’approvazione negli Stati Uniti di un vaccino contro il cancro della prostata basato su cellule dendritiche prelevate dal sangue del paziente e caricate con antigeni. E’ uno solo e con efficacia modesta, però ha mostrato che la macchina volante poteva volare».
ITALIA IN PRIMA LINEA - Qual è il contributo della scuola italiana in questo cammino? «Ahi! Questa domanda apre un conflitto di interessi: l’immunità innata è il mio settore – ride Mantovani -. Nella storia di questi Nobel 2011 ci sono pezzi di ricerca italiana sostenuta da AIRC, magari lontani dalle luci della ribalta, ma indispensabili per lo svolgimento del lavoro. Ad esempio, una linea cellulare di macrofagi usati da Beutler era una linea generata in Italia da Paola Ricciardi-Castagnoli; la scoperta nella drosofila del Toll ha avuto una delle anticipazioni nel settore di Interleuchina 1, a cui ho lavorato anch’io. Un contributo fondamentale all’identificazione dei recettori Toll-like nei mammiferi è stato dato da Marta Muzio nel nostro laboratorio» racconta con orgoglio. «Tutti i dati lo suggeriscono – conclude Alberto Mantovani - l’immunologia è una delle aree più sane e più competitive nel paese».
IL NOBEL? ANCHE UN PO’ LORO - Ma ci sono altri contributi, quelli dei non-premiati che Mantovani tiene a ricordare. E spiega il perché: «Ci sono spesso premi assegnati a persone che sono la punta di diamante di una comunità che ha fatto ricerca. Penso che questo Nobel, giusto e meritatissimo, sia il risultato del lavoro di tanti. Charles Dinarello, con gli studi sull’ interleuchina 1, ha reso possibile il “salto mentale” sul ruolo dei Tlr; Charles Janeway dalla fine degli anni ’80 intuì che la risposta adattiva era regolata da quella innata; un suo collaboratore, Ruslan Medzhitov, ha dimostrato che Toll attivava le cellule dendritiche, Akira Shizuo ha generato varianti genetiche di tutti i recettori Toll-like e le ha condivise con tutti».
UNO SGUARDO AL FUTURO – Dove ci sta portando l’immunologia? «Abbiamo grandi sfide davanti. Ci sono le malattie di classica pertinenza immunologica, quelle in cui il sistema immunitario sbaglia bersaglio. Nelle malattie autoimmuni vari studi hanno consentito di migliorare non poco la qualità di vita dei malati di artrite reumatoide o di patologie infiammatorie dell’intestino, ad esempio. Nelle allergie è cambiato il nostro modo di vedere il rapporto con il mondo microbico (nel nostro corpo ci sono più microrganismi che cellule)».
CACCIA AI POLIZIOTTI CORROTTI - «C’è un’altra sfida: quella di riconvertire e rieducare le difese in situazioni in cui sono state addormentate o alterate. È il caso del cancro, in cui la crescita tumorale trasforma le nostre difese in veri e propri poliziotti corrotti (è la definizione che Mantovani usa nel suo ultimo libro I guardiani della vita, Dalai Editore, ndr). E’ stato approvato un farmaco contro il melanoma che non colpisce le cellule tumorali, ma toglie il freno alla risposta immunitaria. Pochi pazienti ne beneficiano, ma i benefici sono evidenti in termini di sopravvivenza. Mai avuto nulla di simile».
UNA STORIA LUNGA 100 ANNI – Il primo Nobel per la medicina, nel 1901, fu per le terapie con anticorpi. «Per 100 anni si è sognato di usare gli anticorpi per terapie. Con scarsissimi risultati. Ormai nelle terapie contro leucemie, linfomi, tumori del seno, dell’intestino, una grande parte dei nuovi farmaci sono anticorpi. Sono del 1964 i primi tentativi per veicolare un farmaco anticancro tramite un anticorpo, ora l’Fda ha dato la prima approvazione a un farmaco contro il linfoma. E’ l’avverarsi di un sogno che ha richiesto oltre 40 anni per arrivare ai pazienti. E’ stata una rivoluzione silenziosa quella della diagnostica basata sugli anticorpi monoclonali, e diagnosi più accurata significa migliore cura.
L'ULTIMA FRONTIERA - «Un altro obiettivo, non meno importante, che voglio citare è quello della condivisione. Ogni anno 3 milioni di bambini muoiono perché non sono vaccinati con i vaccini più elementari che abbiamo a disposizione. L’Hpv fa 250.000 vittime l’anno, è la prima causa di anni di vita persi per le giovani donne in diverse aree del mondo, come l’Africa sub-sahariana. Il 90% di queste malattie miete vittime nelle regioni più povere del mondo. Credo che gli immunologi per vocazione abbiano il dovere di ricordarsi questa sfida».