Semaforo verde anche in Italia per exa-cel (exagamglogene autotemcel), la prima terapia di editing genetico al mondo basata sulla tecnologia CRISPR-Cas9. AIFA ha da poco dato il via libera alla completa rimborsabilità per tutti i pazienti con beta-talassemia trasfusione-dipendente (TDT) e anemia falciforme severa (SCD) di età pari o superiore a 12 anni. Una novità che riguarda circa 5.000 persone con TDT e 2.300 con SCD, la platea più ampia in Europa. Dopo Stati Uniti, Regno Unito ed Europa, anche in Italia la terapia potrà essere somministrata nei prossimi mesi.
RIPARARE IL GENE "DIFETTOSO"
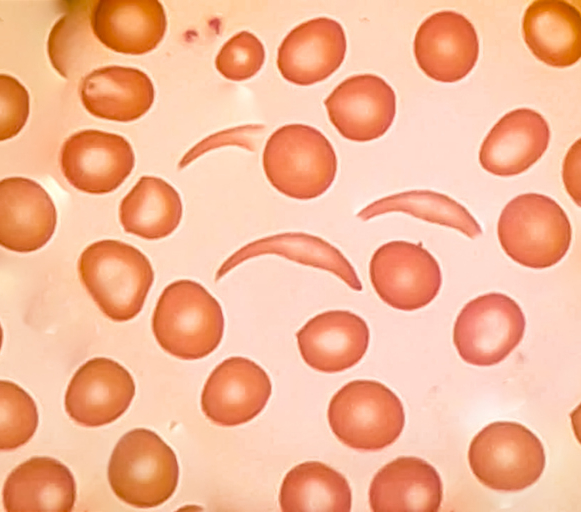
La beta-talassemia e l’anemia falciforme sono malattie genetiche del sangue dovute a difetti nella produzione di emoglobina, la proteina che trasporta l’ossigeno. Nella talassemia, il difetto genetico obbliga i pazienti a ricorrere a trasfusioni periodiche per tutta la vita. Nell’anemia falciforme, i globuli rossi assumono una forma irregolare e fragile che ostruisce i vasi sanguigni e provoca crisi dolorose e danni agli organi. Riparare dunque il difetto genetico alla base delle malattie del sangue è la sola via per non dover più ricorrere a trasfusioni continue.
IL RUOLO DELLA CRISPR
Ed è quello che esattamente fa exa-cel. In questo caso le cellule staminali ematopoietiche del paziente vengono prelevate, corrette in laboratorio grazie alla tecnica CRISPR e reinfuse dopo un ciclo di chemioterapia preparatoria. Una volta attecchite, queste cellule producono emoglobina fetale funzionante, riducendo o eliminando la necessità di trasfusioni nella talassemia e prevenendo le crisi vaso-occlusive nella falciforme. Nei trial clinici che hanno portato all’approvazione, la quasi totalità dei pazienti trattati ha ottenuto una remissione duratura dei sintomi principali.
L’approvazione di exa-cel segna una svolta nella medicina delle malattie genetiche rare. Per la prima volta viene resa disponibile una terapia curativa che non inserisce un gene esterno, ma corregge direttamente quello difettoso. Una strategia che potrebbe allargarsi in futuro ad altre patologie ereditarie.
UNA CURA NON PER TUTTI
Se in Italia e nei Paesi ad alto reddito questa innovazione sarà presto realtà, il quadro globale resta segnato dalle disuguaglianze. Secondo stime pubblicate su The Lancet Haematology, solo il 2% dei pazienti con anemia falciforme vive nei Paesi dove exa-cel potrà essere somministrata, mentre tre quarti dei malati si trovano in aree del mondo prive persino delle cure di base. Qui il problema non è solo il costo – circa 2 milioni di euro per paziente – ma anche la mancanza di infrastrutture per eseguire un trapianto così complesso.
La sfida, dunque, non si esaurisce con l’approvazione della terapia. Riguarda la capacità dei sistemi sanitari di garantire accesso equo alle cure, senza dimenticare che in molte aree del mondo i pazienti continuano a non ricevere neppure farmaci semplici e poco costosi come l’idrossiurea o la profilassi antibiotica.